Berikut ini penjelasan tentang unsur kimia, penggolongan unsur kimia, massa atom, teori atom dalton, hukum triade dobereiner, johann dobereiner, jons jakob berzelius, john alexander reina newlands, hukum oktaf newlands atau hukum oktaf.
Pengelompokan/ Penggolongan Unsur Kimia Berdasarkan Massa Atom
a. Hukum Triade Dobereiner
Pada 1803, John Dalton mengumumkan teori atom dalton. Menurut Dalton:
- semua zat terdiri atas atom yang tidak bisa dibagi lagi;
- semua atom dalam suatu unsur memiliki massa dan sifat yang sama;
- unsur yang berbeda memiliki atom yang berbeda jenisnya dan berbeda massanya; dan
- atom tidak bisa dihancurkan, tetapi susunannya dapat berubah karena suatu reaksi kimia.
Berdasarkan teori atom dalton tersebut, Dalton membuat daftar massa suatu atom. Pada 1828, Jons Jakob Berzelius mengembangkan teori atom yang dikemukakan Dalton.
Dengan diketahuinya massa suatu atom, unsur-unsur kimia mulai dikelompokkan berdasarkan massa atomnya. Ilmuwan yang kali pertama mengelompokkan unsur kimia berdasarkan massa atom adalah Johann Dobereiner.
Pada 1829, ia mengelompokkan unsur-unsur kimia ke dalam suatu kelompok yang terdiri atas 3 unsur yang sifatnya sama.
Ketika diselidiki lebih lanjut, unsur yang kedua memiliki massa atom yang jumlahnya setengah dari penjumlahan massa atom unsur pertama dan unsur ketiga. Dobereiner menamakan pengelompokan unsurnya dengan nama Hukum Triade Dobereiner.
Kelompok unsur-unsur tersebut, yaitu: litium, natrium, dan kalium; kalsium, stronsium, dan barium; belerang, selenium, dan tellurium; klorin, bromin, dan iodin. Benarkah pernyataan yang dikemukakan Dobereiner?
Untuk membuktikannya, ujilah teori Triade Dobereiner tersebut menggunakan tabel massa atom berikut.
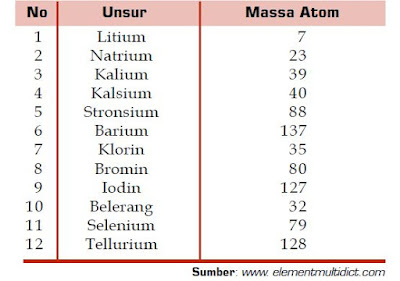 |
| Tabel massa atom beberapa unsur |
b. Hukum Oktaf Newlands
Kimiawan Inggris, John Newlands, menyusun 62 unsur yang saat itu diketahui berdasarkan kenaikan massa atom pada 1864. Unsur-unsur kimia diurutkan dari kiri ke kanan. Gambar berikut ini menunjukkan susunan unsur-unsur kimia yang dikelompokkan Newlands.
 |
| Susunan Unsur-Unsur Kimia Newlands |
Ternyata, kelompok unsur-unsur yang mirip terulang setiap 8 unsur. Jika hitungan diawali dari Li, unsur kedelapan adalah unsur Na dan unsur keenambelas adalah K. Unsur Li, Na, dan K memiliki sifat yang mirip. Begitu juga dengan unsur Be, Mg, dan Ca.
Pengelompokan unsur yang dilakukan Newlands pada 1864 tersebut dikenal dengan nama Hukum Oktaf. Akan tetapi, teorinya ini dianggap hal yang konyol oleh banyak orang. Sampai lima tahun kemudian, Dmitri Mendeleev memperkenalkan suatu bentuk tabel periodik berdasarkan massa atom.







