Berikut ini akan dibahas tentang orbital, pengertian orbital, bentuk-bentuk orbital, bentuk orbital, orbital s, orbital p, orbital d, orbital f, bentuk orbital spdf, bentuk orbital f, bentuk orbital d, bentuk orbital p, bentuk orbital spd, orbital kimia, bentuk bentuk orbital spdf, bentuk molekul, bentuk orbital atom, bentuk bentuk molekul, dan juga bentuk geometri molekul.
Pengertian Orbital
Orbital atom adalah daerah ruang di mana elektron dapat ditemukan. Setiap orbital dapat menampung dua elektron dan orbital yang berbeda memiliki bentuk yang berbeda. Sub kulit s bentuk orbitalnya seperti berbentuk sebuah bola, sedangkan subkulit p memiliki orbital berbentuk tiga dumbbell.
Bentuk orbital ditentukan oleh subkulit dari elektron atau ditentukan bilangan kuantum azimutnya. Jadi, apabila suatu elektron memiliki bilangan kuantum azimut sama,
maka bentuk orbitalnya juga sama, sehingga yang membedakan hanyalah tingkat energinya. Dengan memahami uraian berikut, kalian akan mengetahui bentuk orbital s, p, d, dan f.
a. Bentuk Orbital s
Orbital yang paling sederhana adalah orbital s. Setiap subkulit s terdiri atas 1 buah orbital yang berisi 2 elektron.
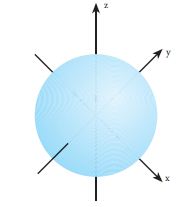 |
| Bentuk orbital s |
Orbital s berbentuk bola simetri yang menunjukkan bahwa elektron memiliki kerapatan yang sama, jika jarak dari inti atom juga sama. Semakin jauh letak elektron dari inti atom, kerapatannya semakin rendah.
Nilai bilangan kuantum utama suatu orbital memengaruhi ukuran orbital. Semakin besar nilai bilangan kuantum utama, ukuran orbitalnya juga semakin besar.
b. Bentuk Orbital p
Bentuk orbital p seperti balon terpilin. Kepadatan elektron tidak tersebar merata, melainkan terkonsentrasi dalam dua daerah yang terbagi sama besar dan terletak pada dua sisi berhadapan dari inti yang terletak di tengah.
 |
| Bentuk orbital Px, Py dan Pz |
Subkulit p terdiri atas 3 orbital, tiap orbital mempunyai bentuk yang sama. Perbedaan ketiga orbital terletak pada arah, dimana terkonsentrasinya kepadatan elektron.
 |
Orbital p digambar menggunakan
satu kumpulan sumbu xyz. |
Biasanya orbital p digambarkan menggunakan satu kumpulan sumbu x, y, dan z, sehingga diberi tanda px, py dan pz.
c. Bentuk Orbital d dan f
Setiap subkulit d terdiri atas 5 orbital dengan bentuk kelima orbital yang tidak sama. Orientasi orbital d dilambangkan dengan dxy, dxz, dyz, dx2-y2 dan dz2.
Empat orbital mempunyai bentuk yang sama dan setiap orbital mempunyai 4 “lobe” kepadatan elektron. Adapun perbedaannya terletak pada arah berkumpulnya kepadatan elektron.
Sementara itu, satu orbital lagi mempunyai bentuk berbeda, tetapi memiliki energi yang sama dengan keempat orbital d lainnya.
Orbital f mempunyai bentuk orbital yang lebih rumit dan lebih kompleks daripada orbital d. Setiap subkulit f mempunyai 7 orbital dengan energi yang setara. Orbital ini hanya digunakan untuk unsur-unsur transisi yang letaknya lebih dalam.







